Un estallido de rápida evolución le permite a Helicobacter pylori, la bacteria que causa úlceras en los seres humanos, evadir el sistema inmune durante la aguda fase temprana de la infección.
Las Helicobacter pylori es una bacteria que infecta el epitelio gástrico humano. Muchas úlceras y algunos tipos de gastritis se deben a infecciones por H. pylori. En muchos casos, los sujetos infectados nunca llegan a desarrollar ningún tipo de síntoma. Esta bacteria vive exclusivamente en el estómago humano, siendo el único organismo conocido que puede subsistir en un ambiente tan extremadamente ácido. Es una bacteria espiral (de esta característica morfológica deriva el nombre de la Helicobacter) y puede «atornillarse» literalmente por sí misma para colonizar el epitelio estomacal.
El nuevo hallazgo complementa un trabajo anterior, que cuantifica con qué rapidez se acumulan las mutaciones de H. pylori durante la infección crónica. Durante la fase aguda, las tasas de mutaciones son 30 a 50 veces mayores que durante la fase crónica.
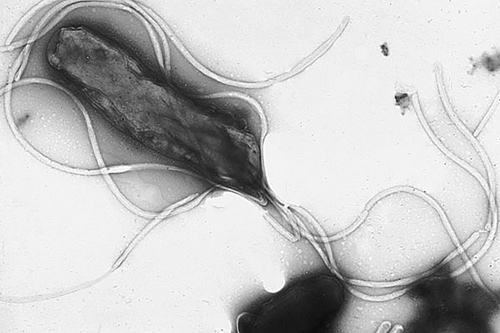
Micrografía electrónica de la bacteria estomacal Helicobacter pylori. (Yutaka Tsutsumi, Escuela Universitaria de Salud Fujita de Medicina)
El estallido de mutaciones fue descubierto por investigadores de la Universidad Estatal de Pensilvania, la Universidad de Australia Occidental y la Universidad de California en Davis. Estos investigadores demostraron, por primera vez, y en tiempo real, la interacción entre el sistema inmune humano y la invasión de las bacterias, que permite que las bacterias contrarresten el sistema inmune mediante una rápida evolución. Los investigadores publicaron sus resultados el 13 de junio en Nature Communications, en un artículo titulado A mutation burst during the acute phase of Helicobacter pylori infection in humans and rhesus macaques («Un estallido de mutaciones estallar durante la fase aguda de la infección por Helicobacter pylori en humanos y macacos rhesus»).
Para rastrear las infecciones de H. pylori en pacientes humanos, los investigadores utilizaron un enfoque de secuenciación de nueva generación. Como indicaron los investigadores en su artículo, analizaron «la tasa y el patrón de la evolución del genoma de H. pylori en los genomas de dos cepas de inicio (entrada) aisladas de voluntarios humanos con infección asintomática, y los genomas de dos cepas de estado final (salida) recogidos 20 y 44 días después de la re-infección.»
También llevaron a cabo un experimento paralelo en un mono rhesus, analizando la «evolución del genoma en bacterias de las secuencias desde el genoma de las cepas de entrada y salida en forma secuencial, tomadas después de la infección experimental de un macaco rhesus». Se recogieron muestras de las bacterias del macaco para secuenciar el genoma en una semana, un mes, dos meses, y seis meses después de la infección inicial.
En el mono, los científicos fueron capaces de comparar directamente la tasa de cambios en el ADN en el genoma de la bacteria entre las fases aguda y crónica. Aunque las mutaciones siguieron acumulándose en el genoma bacteriano durante la fase crónica, la tasa de sustituciones disminuyó considerablemente después del período inicial de cuatro semanas.
«Nos quedamos impresionados por la alta tasa de mutación que nos encontramos en la fase inicial de la infección», dijo Bodo Linz, Ph.D., investigador asociado en Penn State y autor principal del artículo. Los pacientes infectados con H. pylori experimentan una fase inicial aguda de la infección durante el cual los síntomas son más severos y la respuesta inmune es más fuerte.
Una infección con H. pylori provoca una respuesta inmune que implica la liberación de moléculas reactivas de oxígeno y nitrógeno que, se sabe, inducen mutaciones en la secuencia de ADN y causan que los cromosomas se rompan y se recombinen. Los estudios anteriores habían demostrado que el genoma de H. pylori es salvado de este tipo de abuso.
«Las cepas de la bacteria aisladas de diferentes hospederos humanos varían enormemente, tanto en la secuencia de ADN como en el contenido de genes», dijo Stephan Schuster, Ph.D., profesor de bioquímica y biología molecular en la Universidad Estatal de Pensilvania. «Hay alrededor de 1.100 genes centrales que comparten las distintas cepas de H. pylori, pero otros cuatro o cinco centenares de genes varía entre cepas».
«La intensa presión selectiva en las bacterias por sobrevivir a la respuesta inmune, junto con el aumento de las tasas de mutación, produce el ritmo increíblemente rápido de cambio genómico que hemos descubierto en este estudio», agregó el Dr. Linz. «Las mutaciones ocurren al azar en todo el genoma, pero como ayudan a las bacterias a evitar la eliminación por el sistema inmune, los cambios en las proteínas de la membrana externa aparecen mucho más a menudo de lo que cabría esperar para dar chance de sobrevivir a las bacterias».
No se sabe si otras bacterias diferentes de H. pylori se someten a un estallido similar de evolución acelerada inmediatamente después de la infección, pero el equipo planea investigar otros patógenos humanos comunes en la investigación futura.
Fuente: GEN. Aportado por Eduardo J. Carletti
Más información:
- Bacterias activan un escudo para resistir ataques
- Identifican otro mecanismo de comunicación entre bacterias
- Descubren cómo la bacteria "Bacillus subtilis" libera al medio copias de su genoma
- Bacterias producen nanomagnetismo para navegar por los océanos
- Una conocida bacteria que habita nuestro cuerpo puede ser la base para futuros combustibles biológicos