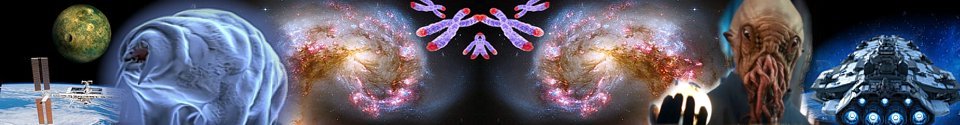
Se trata de un sistema sencillo que permite que unos mini tentáculos puedan sostener objetos a microescala, como huevos de peces, sin romperlos». Este dispositivo robótico de pequeñas dimensiones también podría tener aplicación en dispositivos para la microcirugía, o en aparatos para manipular células o tejidos minúsculos
Hace poco más de un año, la prensa se hacía eco del caso de Dennis Aabo, un danés de 36 años que perdió la mano tras un accidente con la manipulación de fuegos artificiales. Gracias a su participación en un ensayo clínico, se convirtió en el primer amputado del mundo capaz de controlar su prótesis en tiempo real. Con la incorporación de un complejo sistema de sensores, no sólo el cerebro del paciente enviaba señales a la mano biónica para coger, por ejemplo, un vaso, sino que también lograba que la prótesis transmitiera información al cerebro para modular la fuerza necesaria para sostener según el objeto, sin aplastarlo ni romperlo.

Como explican los expertos, las prótesis que se usan hoy en día son muy sencillas. Permiten movimientos muy limitados, abrir y cerrar la mano, por ejemplo. Algunas tienen sensores de temperatura, es decir, cuando el objeto está muy caliente se enciende una luz, pero carecen de un mecanismo que permita la bidireccionalidad de la información. «Aún no sabemos muy bien cómo conseguirlo. Varios equipos de investigadores están trabajando en ello», apunta Eduardo Fernández, investigador de la Universidad Miguel Hernández (Elche, Alicante) y del Ciber-bbn (Centro de Investigación Biomédica en Red Bioingeniería, Biomateriales y Nanomedicina), que también está trabajando en un proyecto similar, en colaboración con un grupo de científicos de la Universidad de Utah (EEUU), con electrodos tridimensionales.
Ahora, la revista Nature presenta un nuevo avance relacionado con el campo de la robótica que quizás pudiera tener aplicación como un sensor capaz de regular la presión que la mano artificial debe imprimir para sujetar objetos delicados. Consiste en un microtubo flexible realizado a partir de material PDMS, un polímero biocompatible, es decir, «no provoca inflamaciones y es tolerado por los tejidos internos del organismo«, aclara Fernández. Esta especie de tentáculo, del grosor aproximado de un cabello, se va enrollando en forma de espiral más o menos a medida que se le inyecta aire. De esta manera, con distintas presiones logra modular su fuerza con la precisión adecuada como para sostener cualquier tipo de insecto, por ejemplo, una hormiga, sin dañar su cuerpo. Así lo demuestra un grupo de científicos de la Universidad de Iowa (EEUU).
Se trata de un sistema sencillo con el que «conseguimos que estos mini tentáculos sostengan objetos a microescala, como huevos de peces, sin romperlos», resume Jaeyoun Kim, principal autor del estudio. Este trabajo robótico de pequeñas dimensiones también podría tener aplicación en dispositivos para la microcirugía o aparatos para manipular células o tejidos minúsculos. Quizás incluso tenga un papel en el trabajo que están desarrollando varios equipos de científicos con el objetivo de diseñar «robots internos con cámara de vídeo. La idea es introducirlos en el cuerpo (a través de pastillas) para que examinen el estado de organismo», señala Fernández. Es posible que, en un futuro, además de esta función, sistemas como el de los tentáculos inventados por Kim logren también manipular o extraer muestras celulares para analizar.
Nanomedicina para el corazón
Otro de los avances ‘micro’ que esta semana sale a la luz, esta vez en la revista Science Translational Medicine, tiene que ver con las nanopartículas. Cuando las arterias coronarias se obstruyen y dan lugar a un infarto o angina de pecho, el bypass es una de las intervenciones quirúrgicas más frecuentes para tratar dichas patologías, consigue mejorar el riego sanguíneo al miocardio. Consiste en utilizar una vena o arteria de otra parte del cuerpo para ‘construir’ un puente entre las zonas sanas de la arteria obstruida. Existen dos tipos: injertos arteriales (de la arteria mamaria o radial) y venosos (de safena, que es una vena de la pierna).
Aproximadamente «la mitad de los injertos venosos empiezan a obstruirse de nuevo a los 12-18 meses tras la operación», argumentan en el artículo los autores del departamento de Ingeniería Biomédica de la Universidad Vanderbilt (EEUU). Generalmente, como resultado de la hiperplasia intimal, engrosamiento de la pared del vaso sanguíneo. Lo que ocurre es que, por estímulos mecánicos, la sangre interacciona con las paredes y va deformándolas. En esta interacción «se van liberando factores inflamatorios en los vasos sanguíneos».
Aunque no siempre es necesario tratarlo, puede producir estenosis por la formación de una nueva placa de ateroma. «Un péptido conocido como MK2i, actualmente en ensayos clínicos, puede bloquear esa liberación de factores inflamatorios», apunta Craig Duvall, uno de los autores del trabajo. Sin embargo, «dicho fármaco se degrada demasiado rápido dentro de las células». Para mejorar la eficacia de MK2i, Brian Evans y su equipo han desarrollado una nanopartícula con carga eléctrica llamada nanopolytex. «Envuelve y transporta el medicamento directamente hasta su objetivo» y con la idea de degradarse a una velocidad adecuada. Después de probarla in vitro sobre células humanas y también en un modelo animal (conejo), se ha visto que las nanopartículas cargadas con el péptido MK2i reducen la hiperplasia intimal, manteniendo la inflamación controlada.
Los resultados sugieren, concluyen los investigadores «que los nanopolyplexes ofrecen un prometedor sistema de administración de fármacos para mejorar la eficacia de la terapéutica de péptidos tales como MK2i para proteger los injertos venosos del fracaso».
Nanopartículas ‘españolas’ para la visión
Un trabajo similar está realizando un grupo de científicos en España, entre los que se encuentra Eduardo Fernández. «Estamos trabajando en nanopartículas (vectores no virales) que transporten material genético al interior de la retina para hacer liberación controlada de ADN» con el objetivo de intentar paliar «enfermedades degenerativas de la retina, como la Degeneración Macular Asociada a la Edad (DMAE) y la retinosis pigmentaria, que son los responsables de casi el 50% de todos los casos de baja visión». Desde la Universidad Miguel Hernández están colaborando con el CIBER-BBN.
Hasta ahora, expone el investigador, una de las formas mas comunes de llevar material genético al interior de las células es utilizar un virus que es modificado para que deje de ser patógeno. Sin embargo esta aproximación «presenta algunos problemas de seguridad y una gran limitación en cuanto al tamaño del material genético a transportar«. En este contexto «nuestro grupo, en colaboración con el Grupo de Tecnología Farmacéutica de la Universidad del País Vasco dirigido por el profesor José Luis Pedraz, trabaja en el desarrollo de nuevos vectores no virales, que puedan ser utilizados para una terapia génica efectiva y segura. El procedimiento es relativamente fácil ya que las nanopartículas son inyectadas directamente dentro del globo ocular y una vez aquí son captadas mediante endocitosis por las células de la retina». Estas nanopartículas incorporan sustancias que protegen el ADN y «moléculas directoras, como la protamina, que permiten dirigirlas hacia el núcleo celular. Además debido a su tamaño nanométrico y a sus múltiples posibilidades de funcionalización es posible facilitar su captación específica por distintos tipos celulares».
Esta nueva forma de terapia génica ha sido probada con éxito en animales. «Creemos que estos resultados son muy prometedores, aunque es evidente que todavía queda mucho trabajo por hacer».
Fuente: El Mundo. Aportado por Eduardo J. Carletti
Más información:
- Flexionando dedos en micro-robótica: científicos del Laboratorio Berkeley crean un potente actuador a microescala
- Las manos del robot alcanzan un toque delicado: tecnología de detección táctil basada en pequeños chips de barómetro
- Un tentáculo robótico de silicona operado neumáticamente
- Un robot blando cambia de color como los pulpos
- Un robot-medusa puede nadar gracias a un tejido que palpita como el músculo cardíaco