Científicos del Bio Architecture Lab (EE UU) han modificado genéticamente la bacteria E. coli para que digiera los azúcares de las algas marrones y las convierta en etanol. De esta manera, las algas podrían ser una fuente rentable de energía, según afirman los autores del proyecto
El petróleo se acaba y la demanda energética sigue creciendo cada día. Por ello se buscan nuevas fuentes económicamente viables. Según los expertos, una de las más firmes candidatas para sustituir a los recursos fósiles son las algas.
“Las algas marrones pueden ser una de las fuentes de biomasa para la producción de combustibles renovables y químicos más sostenibles medioambientalmente”, afirma a SINC Yasuo Yoshikuni del Bio Architecture Lab (BAL). Yoshikuni forma parte del grupo que ha diseñado una bacteria capaz de metabolizar todos los azúcares del alga marina y obtener mayor rendimiento en el proceso.

El equipo del BAL, que publica sus resultados en Science, se basa en dos argumentos para defender este recurso: las algas tienen un contenido muy alto de azúcar y su cultivo no resta agua ni tierra a las cosechas de comida. “La acuicultura a gran escala es benigna con el medioambiente”, asegura Yoshikuni.
Pese a todas las ventajas, hasta ahora no se ha conseguido que esta fuente sea rentable. “La tecnología actual no ha sido capaz de metabolizar todos los azúcares contenidos en el alga”, explica el investigador. “Esto hace que los biocombustibles y los químicos producidos no sean competitivos, respecto a los costes, con los de origen fósil”.
Según los investigadores, el principal problema es la falta de microorganismos manejables que puedan metabolizar polisacáridos del alginato, la sustancia química obtenida del alga. En respuesta a esto, el equipo ha diseñado su propio microbio. “Hemos desarrollado la única plataforma capaz de fermentar prácticamente todos los azúcares de las algas”, informa Yoshikuni.
Ingeniería genética
“Las algas tienen una mezcla de polímeros de azúcar complejos que apenas se encuentran en la biomasa terrestre. Para que se conviertan en una materia prima competitiva hace falta tecnología capaz de metabolizar todos esos azúcares”, expone Yoshikuni.
Con este fin, el equipo del BAL ha modificado el ADN de la bacteria E. Coli de manera que codifique las enzimas necesarias para transportar y metabolizar el alginato. Lo han integrado en el genoma del microorganismo y así han generado una plataforma que puede degradar, captar y metabolizar el ácido.
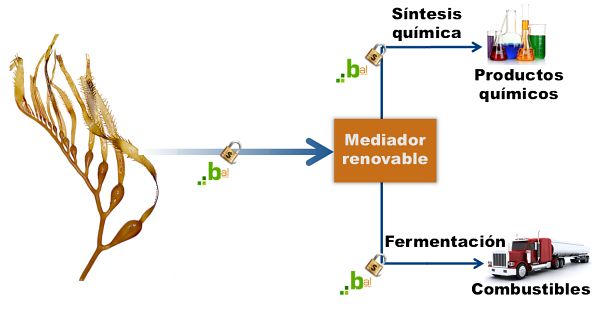
A partir del ácido, la bacteria sintetiza etanol a través un proceso que ya se utiliza. “La diferencia es que se consigue metabolizar el equivalente al 80% del rendimiento máximo teórico del azúcar contenido en el alga”, señalan en el artículo.
Pero todavía faltan mejoras en este desarrollo. “Son necesarias innovaciones en las encimas secretadas que digieren el azúcar, también en las proteínas de membrana que transportan los oligosacáridos y en los procesos metabólicos que fermentan los azúcares y los convierten en combustibles renovables y químicos”, advierte Yoshikuni.
Algas macroscópicas
En el este proyecto se utilizaron macroalgas de la especie kombu (Saccharina japonica), que es la más abundante y extendida en todo el mundo. “Tiene propiedades claves para convertirse en una excelente materia prima: no requiere terrenos cultivables, ni fertilizantes, ni agua dulce, y además reduce mucho la emisión de CO2”, aseguran en el artículo.
La mayoría de los estudios se realizan con algas microscópicas, debido a su menor complejidad estructural, mayor ritmo de crecimiento y alto contenido en aceite. Sin embargo, la mayor disponibilidad de macroalgas hace que algunas investigaciones opten por estos organismos.
BAL ya está construyendo la instalación piloto en Chile para mostrar con más precisión el coste total de proceso a gran escala. Las operaciones comenzarán en julio.
Referencia bibliográfica: A.J. Wargacki; E. Leonard; M.N. Win; D.D. Regitsky; C.N.S. Santos; P.B. Kim; S.R. Cooper; R.M. Raisner; A. Herman; A.B. Sivitz; A. Lakshmanaswamy; Y. Kashiyama; Y. Yoshikuni, Y. Kashiyama, D. Baker, A. Herman, A.B. Sivitz. «An Engineered Microbial Platform for Direct Biofuel Production from Brown Macroalgae«. Science, 335. 20 de enero de 2012.
Fuente: Sinc. Aportado por Eduardo J. Carletti
Más información:
- Una conocida bacteria que habita nuestro cuerpo puede ser la base para futuros combustibles biológicos
- Árboles que emiten luz podrían iluminar las calles
- Carne producida en laboratorios
- Crean en China una hoja artificial que produce energía
- Circuito eléctrico funciona con suministro de energía de los árboles
- Dicen que EEUU podría solucionar el problema de los combustibles fósiles usando torio
- Una compañía japonesa quiere convertir la Luna en una planta solar gigante
- Científicos logran robar electrones de la fotosíntesis de las algas
- NASA: Cultivos para energía alternativa en el espacio
- Una nanomáquina biológica logra plegar proteínas